1. 上海之江生物科技股份有限公司的一款针对新冠病毒的双特异性抗体药物SYZJ001,目前已经完成了全部的临床前研究,将进入临床前申请阶段。
据悉,之江生物于2020年初与参股公司上海三优生物共同组建团队,合作开发了SYZJ001。这是我国原创研发的抗新冠病毒治疗药物,也是全球研发进展较为领先的双特异性抗体药物。
之江生物总经理吕力琅表示,在实验室内对新冠病毒的突变株进行的临床前研究表明,SYZJ001对各类突变株的中和效果都非常好,尤其对现在全球比较普遍的Delta,也体现出了很好的中和效果。
吕力琅说:“如果获得一期临床批件,我们将开展在人体的一期临床实验。
上海之江生物科技股份有限公司(688317.SH,下称“之江生物”) 的一款针对新冠病毒的双特异性抗体药物SYZJ001,目前已经完成了全部的临床前研究,将进入临床前申请(Pre-IND)阶段。
11月6日,在第四届中国国际进口博览会上,勃林格殷格翰和之江生物共同宣布,将由勃林格殷格翰为SYZJ001提供生产工艺开发及优化、原液和制剂cGMP生产,以及CMC申报文件支持等服务。
上海之江生物科技股份有限公司总经理吕力琅对第一财经表示,目前SYZJ001已经完成了全部的临床前研究,“该项目已正式进入中、美新药I期临床试验申请前沟通交流(Pre-IND)程序,如果获得一期临床批件,我们已经做好了开展在人体的一期临床实验的准备。”
2. 全球研发进展较为领先的双抗药物
美东时间11月5日,辉瑞发布消息称,其研究性新型COVID-19口服抗病毒候选药物PAXLOVID的2/3期研究的中期分析显示,PAXLOVID与低剂量的利托那韦共同使用,与安慰剂相比,患有COVID-19的非住院高危成人的住院或死亡风险降低89%。
辉瑞公司首席科学官MikaelDolsten表示,辉瑞计划在11月争取美国食品药品监督管理局(FDA)批准该药物,如果获批,PAXLOVID可能在今年交付市场。
11月4日,默沙东的新冠口服药Molnupiravir在英国市场获批上市,根据研究结果,与安慰剂相比,Molnupiravir能降低患者住院或死亡风险约50%。
吕力琅说,全球都很关注新冠治疗的药物,目前基本都是单抗药物,SYZJ001是一个大分子的双抗药物。“就像疫苗开发有很多不同的技术路线,抗击新冠的药物也有不同的技术路线,我们对SYZJ001的中和能力特别是防突变能力,是非常有信心的。”
之江生物于2020年初与参股公司上海三优生物共同组建团队,合作开发了SYZJ001,这是我国原创研发的抗新冠病毒治疗药物,也是全球研发进展较为领先的双特异性抗体药物。
SYZJ001由靶向新冠病毒Spike蛋白受体结合结构域(RBD)的全人源IgG抗体分子和人源化纳米抗体分子构成,两个抗体可互不竞争地结合RBD蛋白的抗原表位,分别阻断病毒与人体ACE2受体的结合,高效中和新冠病毒感染入侵细胞。
其中,纳米抗体分子P14-F8对目前主流突变株及主要突变位点均未逃逸,对Delta毒株和Epsilon毒株的中和活性相比于野生型毒株增强。与全人源IgG抗体分子组成双抗后,不但具有优异的新冠病毒中和活性,还具有更广谱的防感染特性,可广泛中和新冠病毒突变株及防止突变逃逸,其有效性已在细胞水平实验和小鼠体内模型上得到验证。尤其对于Delta突变株,SYZJ001保持了与野生型毒株相似的中和效果。前期动物实验结果也表明SYZJ001安全性良好。
“前期从蛋白水平到细胞水平,包括在小鼠体内的药效认证,都得到了非常好的效果。安全性也非常好。”同时,吕力琅说,在实验室内也对新冠病毒的突变株进行了临床前研究,证实SYZJ001对各类突变株的中和效果都非常好,尤其对现在全球比较普遍的Delta,也体现出了很好的中和效果。
“我们希望它能够顺利走向临床研究,一直到未来上市。” 吕力琅说。
3. 选择CDMO模式
SYZJ001是之江生物目前在生物医药领域布局的全新战略重点,不过,因为之江生物不具备药物生产能力,于是选择了生物制药合同开发与生产(CDMO)的模式。
吕力琅说,希望通过与勃林格殷格翰的合作,共同为临床供应质量稳定可靠的药品。同时期待产品顺利面世,继续进行深度商业化合作。
对勃林格殷格翰而言,这也是其位于上海张江的生物制药业务二期扩建竣工后落地的首个战略合作伙伴。中国上海、德国比伯拉赫、奥地利维也纳、美国加利福尼亚,是勃林格殷格翰全球四大生物制药基地之一。上半年二期扩建后,勃林格殷格翰位于上海生产基地的生物制药产能达到6000公升,是建成之初的3倍。
目前,中国生物医药行业步入发展快车道,合同生产业务的市场需求持续增加。
勃林格殷格翰是首个在中国建立国际化生物制药基地的跨国药企。作为《药品上市许可持有人制度试点方案》中唯一一个生物制药合同开发生产试点项目,勃林格殷格翰生物制药基地自2017年启用以来,已经为多家国内创新药企和全球顶尖跨国制药企业提供了合同生产业务。其中就包括2019年底获批上市的百济神州自主研发的PD-1抑制剂替雷利珠单抗,这也是国内首个上市许可持有人采用合同生产模式获得上市批准的创新生物药。
10月11日,勃林格殷格翰(BI)宣布成为上海世界级生物医药产业集群共建伙伴,未来将通过CDMO,赋能创新药物“上海研发,上海制造”,走向全球。
“这几年上海创新药的数量持续增长,相应的生产许可证数量达到27张,显示CDMO可以极大激发创新药的研发上市进程,也改变了研发企业卖青苗的现象。”勃林格殷格翰生物药业(中国)有限公司总经理王彬对第一财经表示。
王彬说,在美国和欧洲等成熟市场,制药企业生产外包比例已占整个生产过程的20%。中国的CDMO业务发展还处于早期飞速扩展的阶段,但发展的大方向非常明确。
董事火速增持
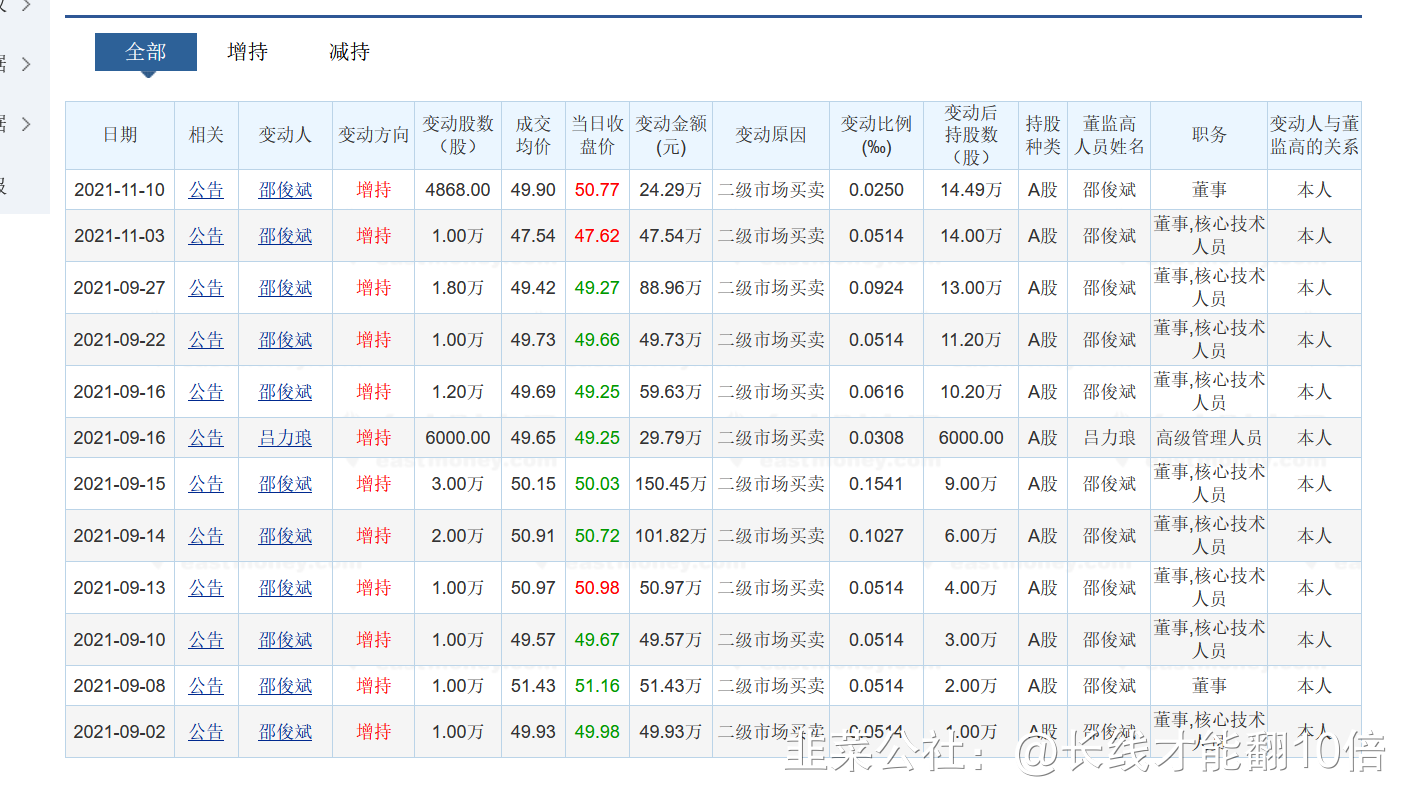
我买了半仓
上述文章仅供参考,不作为买入信号,入市有风险,炒股需谨慎。



- 1
- 2











