中国第一款进入注册申报阶段的3D打印药物产品。
天士力可能占比三迭纪约7.14%
:天士力在pre-A轮向三迭纪投资1500万元,其中37.5万元计入注册资本(投后注册资本367.5万元,投后估值1.47亿元);2018年6月2日,三迭纪完成了1亿元人民币A轮融资(投后估值4.21亿元)。目前三迭纪注册资本524.82万元,天士力占比约7.14%。从三迭纪产品命名为T19与天士力T89类似来看,未来三迭纪与天士力可能不仅仅是财务投资关系,可能存在深入合作的可能
资源库7月1日丨近日,南京三迭纪医药科技有限公司(简称“三迭纪”,英文名Triastek)宣布,该公司自主研发的3D打印药物产品T19已获得国家药品监督管理局(NMPA)核准签发的《药物临床试验批准通知书》。这是三迭纪在NMPA获批的第一个IND,也是中国第一款进入注册申报阶段的3D打印药物产品。

打开APP,查看更多精彩图片
三迭纪T19获NMPA临床试验批准,图片来自:国家药品监督管理局药品审评中心
T19是三迭纪自主设计开发的具有全球知识产权的3D打印药物。该药物的适应症为甲氨蝶呤疗效不足或对其无法耐受的中度至重度活动性类风湿关节炎(RA)成年患者,可与甲氨蝶呤或其他非生物改善病情抗风湿药(DMARD)联合使用的枸橼酸托法替布延迟缓释口服片剂。
患者睡前服用T19,血液中的药物浓度在疼痛、关节僵硬及功能障碍等疾病症状最严重的早晨达峰,并维持其日间血药浓度,从而取得最佳的药物治疗效果。
3D打印药物制剂公司三迭纪获1亿元A轮融资
2018年06月07日
11393次阅读
观察
前瞻产业研究院
扫码阅读

当3D打印技术刚刚萌芽的时候,许多人对它持怀疑态度。但是随着科技发展的需求。现在,它已经变得越来越常见、越来越普及了。如今,3D打印药物的出现,为我们创造了按需制药的可能性。6月4日消息,三迭纪医药科技有限公司近日完成1亿元人民币A轮融资,本轮融资由晨兴创投领投,火山石投资及华新基金共同参与投资。
据悉,本轮融资资金将用于支持公司开发规模化生产药物3D打印设备,推进3D打印药物产品的临床前和临床研究。
三迭纪于2015年7月成立,致力于搭建全新的热熔沉积(FDM)3D打印药物制剂开发和生产技术平台,技术覆盖药物剂型设计、药物生产设备、药物产品生产工艺等多方面,2016还曾获得天士力医药领投的Pre-A轮融资。
公司首创FDM药物3D打印生产技术,自主研制了全球第一台高通量FDM药物专用3D打印机,通过多打印头联动和关键参数反馈控制系统等设计,实现了众多药用物料的高速率、高精度、高通量打印,以及制剂生产一次成型、产品质量实时控制的全新药物连续化生产模式。
目前,三迭纪拥有国内外专利申请36项,自主研发的首个3D打印药物产品将于年内在美国进入临床研究阶段。
3D打印能够完美制造出大剂量、可快速溶解的药丸,而这对于医生来说无疑是一大福音——这就相当于对药物生效的速度和药物效果的强弱有了完全的控制权,医生将能够根据自己的实际需要来对药物进行私人定制。
这项技术有望彻底改变药品制造行业的规则,为医药行业带来多种可能性。用这项技术制造出来的药物可在一定的时间间隔内释放剂量,还可把一整天的药物剂量全压缩到一颗药丸之中。这将为患者带来极大的便利性。另外,3D打印制造药物所需的成本也比现有技术低得多,而且它完全可以根据你的需求来加以制造。
对于此次投资,晨兴创投董事总经理薛文煜表示:“作为一家专注于早期生物科技投资的基金,晨兴创投在全球发掘具备颠覆性创新潜力的平台技术。南京三迭纪开发的热熔沉积3D打印药物技术,将有机会变革从制剂研发到生产的全流程,给患者提供更多、更好的药物选择。很高兴有机会和南京三迭纪团队合作,加速推进平台及在研药物的开发。”
中国首款3D打印药物产品三迭纪T19获NMPA药物临床试验(IND)批准
2022-07-01 15:23
近日,南京三迭纪医药科技有限公司(简称“三迭纪”)宣布公司首个3D打印药物产品T19获得国家药品监督管理局(NMPA)的药物临床试验(IND)批准。该产品在中国按照2.2类改良型新药进行注册申报,是已知公开的首个在中国获得IND批准的3D打印药物产品。
© 国家药品监督管理局药品审评中心官网
T19是三迭纪自主设计开发的具有全球知识产权的3D打印药物。该产品根据时辰治疗学原理,针对类风湿性关节炎症状的昼夜节律进行设计。患者睡前服用T19,血液中的药物浓度在疼痛、关节僵硬及功能障碍等疾病症状最严重的早晨达峰,并维持其日间血药浓度,从而取得最佳的药物治疗效果。
类风湿性关节炎在美国、中国等主要市场国家均有着巨大的临床和市场需求,到2025年预计全球市场规模将达到307亿美元(CAGR 4.5%)。根据中美临床关键意见领袖(KOL)访谈意见,晨间症状仍然是困扰类风湿性关节炎患者的主要问题,而T19独特的时辰治疗优势将为患者提供更好的临床用药选择。
此前,T19在美国FDA通过505(b)(2)路径进行注册申报,于2021年获得IND,是已知公开的全球第二款在美国FDA注册申报的3D打印药物产品。该产品接下来将分别在美国和中国开展临床研究,并向FDA和NMPA递交上市申请(NDA)。
三迭纪创始人、首席执行官成森平博士表示:T19产品在中国获得IND批准,是T19国际注册的一个里程碑。在审评和沟通过程中,三迭纪感受到了CDE对于新兴制药技术的鼓励和支持。三迭纪基于3D打印的连续化制剂生产技术,响应国家“十四五”医药工业发展规划对于提升高端制剂生产技术、推动医药制造能力系统升级的方向指引。未来,三迭纪将用先进的制药技术为中国患者带来更优临床价值和更高产品质量的药物。
知之既深,行之则远。基于全球范围内精湛的制造业专家智囊网络,3D科学谷为业界提供全球视角的增材与智能制造深度观察。有关增材制造领域的更多分析,请关注3D科学谷发布的白皮书系列。
天士力参股公司三迭纪3D打印重磅药物获美国FDA临床试验(IND)批准
来自不灭的火88的雪球专栏
火兄注:三迭纪是天士力参股公司,是天士力在pre-A轮投资的企业,这说明公司的投资眼光是不错的。不知道天士力有没有三迭纪相关产品的国内销售权益。
近日,南京三迭纪医药科技有限公司(简称“三迭纪”,英文名Triastek)宣布,该公司自主研发的3D打印药物产品T20已获得美国FDA的临床试验批准(IND)。这是三迭纪在FDA获批的第二个IND,也是全球第三款进入注册申报阶段的3D打印药物产品。

三迭纪的T20在美国FDA的注册申报路径是505(b)(2),原研产品从2018年起连续四年为全球小分子药物销售冠军。原研产品为速释片,需要一天服用两次,临床疗效包括降低非瓣膜病性房颤患者的卒中和全身性栓塞风险、预防和治疗深静脉血栓(DVT)和肺栓塞(PE)等。美国临床关键意见领袖表示:如果将一天两次服用的药物改为一天一次,可以减轻房颤患者用药负担,提高预防DVT和PE患者的依从性,降低血栓发生风险,从而为患者提供更好的临床用药选择。
公开信息显示,原研公司尝试过多种技术手段来开发一天一次的制剂产品,其专利公布了与速释制剂相比,同样剂量一天一次调释制剂的相对生物利用度只有50~70%,达峰后浓度快速下降。其主要原因在于,一天一次日剂量下此药物的溶解度很低,并且随着肠道转运至远端小肠和升结肠后,药物的渗透性也大幅降低,难以被有效吸收。此药物的低溶解度和体内低渗透性对开发一天一次的产品,带来了很大的技术挑战。
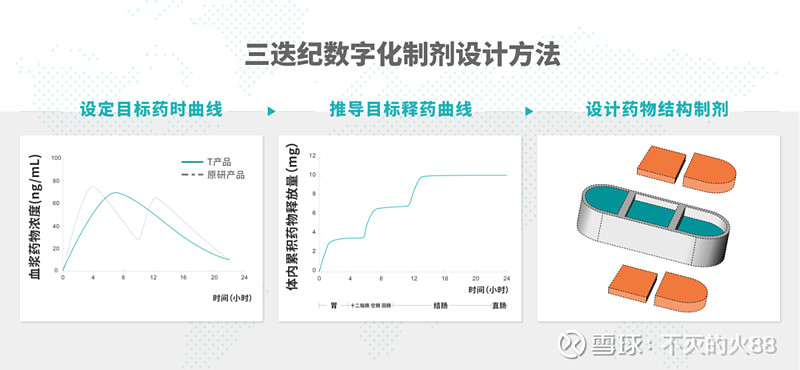
三迭纪创新的数字化制剂开发方法和独有的程序化释药技术,给只需服用一天一次的T20产品的开发提供了技术解决方案,以期达到传统制剂技术难以实现的药物代谢动力学曲线。三迭纪开发了3D打印剂型源于设计(3D Printing Formulation byDesign, 3DFbD®)的数字化制剂开发方法,首先根据优化的目标药代动力学曲线,应用基于生理学的生物药剂学模型,根据文献人体参数,计算出体内不同时间和空间的目标释放曲线;然后根据该目标释放曲线,使用热熔挤出沉积(Melt Extrusion Deposition, MED®)3D打印技术,设计并制备含有多腔室的药物结构制剂,实现释药的“3R”精准控制,即药物在正确的时间(Right time),以正确的剂量(Right amount),递送到人体正确的胃肠道部位(Right location),使得药物被有效吸收。三迭纪研发的T20产品原型,已经在比格犬体内得到了验证,下阶段将推进小规模临床药代动力学研究。
2021年在完成前期可行性研究后,三迭纪向美国FDA递交了T20的PIND会议申请,得到了FDA有关产品开发计划的积极正面的回复。FDA同意,通过临床药代动力学研究与原研建立桥接关系,T20即可申报上市,因此产品开发的时间和成本显著减少。
三迭纪定位为3D打印制剂技术平台型公司,具有自主研发产品和合作开发产品并行的商业模式。其自主开发的全球T系列产品为505(b)(2)药物,原研均为该疾病领域在售重磅小分子药物,三迭纪运用独特的程序化释药技术对其进行产品改良,并对外许可其全球商业权力。作为拥有原创技术的新兴制药科技公司,三迭纪的全球T系列产品肩负着将MED 3D打印技术用于药物产品开发、国际申报注册、GMP生产、商业化,以及实现公司全球化的使命。此外,三迭纪基于专有的3D打印制剂技术平台,已经和多家跨国药企及国内药企合作,共同开发具有高难度制剂技术的505(b)(1)产品,以及具有高度差异化的505(b)(2)产品。

T20是三迭纪自主研发的全球T系列产品中的第二款,原研为全球最畅销的抗凝血药物,化合物在美国、欧洲、日本等主要市场国家和地区仍在专利保护期,全球市场销售预期将持续攀升,年销售峰值预估高达220亿美元。作为原研生命周期管理的新一代改良型产品,T20将积极探索产品商业许可的机会,并将根据商业合作推进国际注册申报和临床研究进程。
三迭纪创始人、CEO成森平博士说:“新兴制药技术从开发到应用,通常需要30年,3D打印制药已经走过26年。目前,全球共有四款注册申报的3D打印药物产品,三迭纪有幸贡献了其中三款。T20获得FDA的IND,既是三迭纪的里程碑,也是3D打印制药领域的重要进展。”
$恒瑞医药(SH600276)$ $信立泰(SZ002294)$ $贝达药业(SZ300558)$
















